Back Alleenpaar Afrikaans زوج غير رابط Arabic Slobodni elektronski par BS Lonepair Danish Freies Elektronenpaar German Lone pair English Par solitario Spanish جفت الکترون غیرپیوندی Persian Vapaa elektronipari Finnish Doublet non liant French
En química, un parell solitari es refereix a un parell d'electrons de valència que no es comparteixen amb un altre àtom en un enllaç covalent[1] i de vegades s'anomena parell no compartit o parell no enllaçant. Els parells solitaris es troben a la capa d'electrons més externa dels àtoms. Es poden identificar mitjançant una estructura de Lewis. Per tant, els parells d'electrons es consideren parells solitaris si dos electrons estan aparellats però no s'utilitzen en l'enllaç químic. Així, el nombre d'electrons en parells solitaris més el nombre d'electrons en enllaços és igual al nombre d'electrons de valència al voltant d'un àtom.
El parell solitari és un concepte utilitzat en la teoria de repulsió de parells electrònics de la capa de valència (teoria VSEPR) que explica les formes de les molècules. També es fa referència a la química dels àcids i bases de Lewis. Tanmateix, no tots els parells d'electrons no enllaçats són considerats pels químics com a parells solitaris. Alguns exemples són els metalls de transició on els parells no enllaçats no influeixen en la geometria molecular i es diu que són estereoquímicament inactius. En la teoria dels orbitals moleculars (orbitals canònics totalment deslocalitzats o localitzats d'alguna forma), el concepte d'un parell solitari és menys diferent, ja que la correspondència entre un orbital i els components d'una estructura de Lewis sovint no és senzilla. No obstant això, els orbitals ocupats no enllaçants (o orbitals de caràcter majoritàriament no enllaçants) s'identifiquen amb freqüència com a parells solitaris.
-
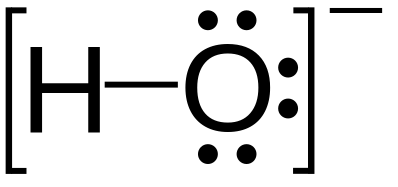
Parells solitaris (mostrats com a parells de punts) a l'estructura de Lewis de l'hidròxid
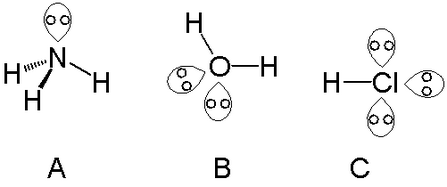
Es pot trobar un parell solitari amb àtoms del grup del nitrogen, com el nitrogen de l'amoníac. Es poden trobar dos parells solitaris amb àtoms del grup del calcogen, com l'oxigen a l'aigua. Els halògens poden portar tres parells solitaris, com el clorur d'hidrogen.
En la teoria VSEPR, els parells d'electrons de l'àtom d'oxigen a l'aigua formen els vèrtexs d'un tetraedre amb els parells solitaris en dos dels quatre vèrtexs. L'angle d'enllaç H–O–H és de 104,5 °, inferior als 109 ° predits per a un angle tetraèdric, i això es pot explicar per una interacció repulsiva entre els parells solitaris.[2][3][4]
S'han proposat diversos criteris computacionals per a la presència de parelles solitàries. Tot i que la densitat electrònica ρ(r) en si mateixa generalment no proporciona una guia útil en aquest sentit, el laplacià de la densitat electrònica és revelador, i un criteri per a la ubicació del parell solitari és on L(r) = –∇2ρ(r) és un màxim local. Els mínims del potencial electroestàtic V(r) és un altre criteri proposat. Un altre considera la funció de localització d'electrons (ELF).[5]
- ↑ «Definition: lone (electron) pair» (en anglès). Gold Book (IUPAC).
- ↑ Fox i Whitesell, 2004.
- ↑ McMurry, 2000.
- ↑ Lee, 1968.
- ↑ Kumar et al., 2014, p. 526-532.