
Back Β-Fass German Beta barrel English Barril beta Spanish Tonneau bêta French Barril beta Galician Barile β Italian Βバレル Japanese Бета-цилиндар Macedonian Bèta-barrel Dutch Barril beta Portuguese



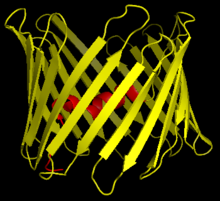
En beta-barrel er den almindelige betegnelse for en protein-struktur, på dansk en beta-tønde, der er et beta-sheet formet som en cylinder og som derved danner en lukket struktur, hvor den første beta-tråd er bundet til den sidste beta-tråd med hydrogenbindinger. Beta-tråde i beta-tønder er typisk arrangeret som antiparallelle peptidkæder.[1]
Tøndestrukturer forekommer i bakterier, mitokondrier og grønkorn som membranproteiner (poriner, der tillader molekyler at passere membranen) og i bakterie og eukaryoter som calyciner, en strukturel superfamilie af proteiner, der binder og transporterer hydrofobe molekyler: lipocaliner (ligand-bindende proteiner klassificeret som transportproteiner), FABP (fedtsyre-bindende proteiner) og avidiner (binder biotin, vitamin B7. Tønde-strukturer som poriner udgør 2-3% af generne i Gram-negative bakterier. Det enestående sammenfald, at membranproteiner med beta-barrel-struktur kun er fundet i bakterier, mitokondrier og grønkorn, leverer et stærkt indicium på at mitokondrier og grønkorn er opstået ved symbiose mellem en bakterie og en celle.