
Back Isomeer Afrikaans تصاوغ Arabic সমাণু Bengali/Bangla Izomeri BS Isòmer Catalan ئایزۆمەر CKB Isomer Welsh Isomer German Isomer English Izomero Esperanto
Indenfor kemi beskriver betegnelsen isomer en af to eller flere kemiske forbindelser, der har samme molekylformel (grundstofindhold), men forskellig opbygning. Isomerer har således forskellige strukturformler. Mange isomerer har identiske eller lignende kemiske egenskaber, men de kan også være forskellige. Isomerer kan desuden have samme eller forskellige fysiske egenskaber.
Et eksempel er de tre isomerer som har molekylformlen C3H8O:
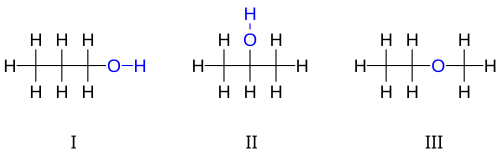
De tre strukturformler indeholder samme antal atomer, men atomerne er sat sammen på forskellige måder. Struktur I er en primær alkohol 1-propanol. Struktur II er også en alkohol, den er dog sekundær og hedder 2-propanol. Forskellen mellem de to strukturer er hvor på kulstofkæden alkoholgruppen (-OH) sidder.
Struktur III viser en helt anden kemisk forbindelse end de to første, nemlig en æter. Selvom denne kemiske forbindelse har samme grundstofindhold som de to førstnævnte har den vidt forskellig kemiske egenskaber, idet iltatomet er bundet til to kulstofatomer, og ikke et kulstof- og et brintatom.
Ikke alle kemiske forbindelser har isomerer. De med få atomer, har ofte ingen eller få isomerer, mens antallet at isomerer stiger hurtigt jo flere atomer der er.