
Back Gebluste kalk Afrikaans هيدروكسيد الكالسيوم Arabic Kalsium hidroksid Azerbaijani کلسیوم هیدروکسید AZB Калциев хидроксид Bulgarian ক্যালসিয়াম হাইড্রোক্সাইড Bengali/Bangla Kalcij-hidroksid BS Hidròxid de calci Catalan Hydroxid vápenatý Czech Кальций гидроксичĕ CV
| Hydroxyde de calcium | |
| |
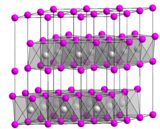
| Structure cristalline. __ Ca2+ __ OH− |
|
| Identification | |
|---|---|
| Synonymes |
dihydroxyde de calcium, |
| No CAS | |
| No ECHA | 100.013.762 |
| No CE | 215-137-3 |
| PubChem | 14777 |
| No E | E526 |
| SMILES | |
| InChI | |
| Apparence | cristaux incolores ou poudre blanche[1] |
| Propriétés chimiques | |
| Formule | Ca(OH)2 |
| Masse molaire[2] | 74,093 ± 0,005 g/mol H 2,72 %, Ca 54,09 %, O 43,19 %, |
| Propriétés physiques | |
| T° fusion | (décomposition) : 580 °C[1] |
| Solubilité | 1,85 g·L-1 (eau, 0 °C) 1,73 g·L-1 (eau, 20 °C) |
| Masse volumique | 2,24 g·cm-3[3] |
| Cristallographie | |
| Système cristallin | Trigonal |
| Réseau de Bravais | Hexagonal |
| Paramètres de maille | a = 3,589 Å c = 4,911 Å Z = 1 |
| Volume | 54,69 Å3 |
| Précautions | |
| SIMDUT[4] | |
 E, |
|
| Transport | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|

L'hydroxyde de calcium est un corps chimique minéral, composé ionique du cation calcium et de l'anion hydroxyde, de formule brute Ca(OH)2. Cet alcali antique est aussi appelé « chaux éteinte », « chaux grasse » et « chaux aérienne », car cette poudre corrosive et hygroscopique était préparée à partir de la chaux vive ou oxyde de calcium produite autrefois par le four à chaux du chaufournier. C'est également un minéral naturel rare, de densité 2,23, nommé « portlandite » par les minéralogistes car il s'agit d'un simple produit d'hydrolyse du ciment Portland.
Il s'agit du principal constituant dissous de l'eau de chaux ou en suspension du lait de chaux. En effet, ce minéral hydroxyde alcalino-terreux est très peu soluble dans l'eau : suivant la composition des chaux éteintes industrielles, souvent un peu magnésiennes, entre 1,1 g·L-1 et 1,6 g·L-1 à 20 °C, environ entre 0,6 g·L-1 et 0,7 g·L-1 à 80 °C[5]. Le composé pur au laboratoire est à peine légèrement plus soluble[6]. Sa solubilité déjà très faible dans l'eau décroît faiblement avec la température. Sa constante de produit de solubilité est de l'ordre de 5,02 × 10−6 à 25 °C.
- HYDROXYDE DE CALCIUM, Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « Calcium hydroxide » dans la base de données Hazardous Substances Data Bank (consulté le 21 septembre 2009).
- « Hydroxyde de calcium » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Pour le produit pur de laboratoire, la solubilité dans l'eau avoisine 1,85 g·L-1 à 0 °C ; 1,28 g·L-1 à 50 °C ; 0,71 g·L-1 à 100 °C.
- Infobox