
Back لوموستين Arabic لوموستین AZB Lomustina Catalan Lomwstin Welsh Lomustin German Lomustine English Lomustina Spanish لوموستین Persian Lomustiini Finnish לומוסטין HE
| Lomustine | ||
| ||
 | ||
| Identification | ||
|---|---|---|
| Synonymes |
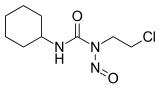
1-(2-chloroéthyl)-3-cyclohexyl-1-nitrosourée (CCNU) |
|
| No CAS | ||
| No ECHA | 100.032.585 | |
| DrugBank | DB01206 | |
| PubChem | ||
| InChI | ||
| Propriétés chimiques | ||
| Formule | C9H16ClN3O2 |
|
| Masse molaire[1] | 233,695 ± 0,012 g/mol C 46,26 %, H 6,9 %, Cl 15,17 %, N 17,98 %, O 13,69 %, |
|
| Propriétés physiques | ||
| T° fusion | 90 °C | |
| Données pharmacocinétiques | ||
| Biodisponibilité | ~100% | |
| Liaison protéique | 50% | |
| Demi-vie d’élim. | 16–48 hours (metabolites) | |
| Considérations thérapeutiques | ||
| Voie d’administration | per os | |
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
La lomustine est un nitrosourée alkylant utilisé en chimiothérapie. Elle est chimiquement très proche de la sémustine et appartient à la même famille que la streptozotocine. C'est une molécule très liposoluble[2], qui traverse donc bien la barrière hémato-encéphalique. Cette propriété la place au 1er plan pour le traitement des tumeurs cérébrales, des gliomes, et des glioblastomes multiformes, ses principales indications, bien qu'également utilisée dans le traitement du lymphome de Hodgkin en deuxième intention[3].
Contrairement à la carmustine, la lomustine est administrée par voie orale. C'est un agent alkylant bifonctionnel, alkylant à la fois l'ADN & l'ARN, et a la capacité de créer des liaisons croisées interbrins dans l'ADN[4].
Comme d'autres nitrosourées, elle peut également inhiber plusieurs processus enzymatiques clefs par carbamoylation des acides aminés[5]. La lomustine est non spécifique du cycle cellulaire.
Elle est hydroxylée dans le foie en trans-4-hydroxy-lomustine & cis-4-hydroxy-lomustine[6].
Elle a également été utilisée dans la médecine vétérinaire dans le traitement des mastocytomes chez le chien[7].
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « BC Cancer Agency Cancer Drug Manual. Lomustine (CCNU; CeeNU) »
- « PRODUCT INFORMATION CeeNU(lomustine) », sur TGA eBusiness Services, Bristol-Myers Squibb Australia Pty Ltd,
- Principles and Practice of Pediatric Oncology, Lippincott Williams & Wilkins, (ISBN 9780781754927), p. 300
- NextSource Biotechnology, LLC, « Gleostine (lomustine) Capsules, for Oral Use. Full Prescribing Information »
- Lee FY, Workman P, Roberts JT, Bleehen NM, « Clinical pharmacokinetics of oral CCNU (lomustine) », Cancer Chemotherapy and Pharmacology, vol. 14, no 2, , p. 125–31 (PMID 3971475, DOI 10.1007/bf00434350, S2CID 29619378)
- Douglas J. Weiss, Jane K. Wardrop, Schalm's Veterinary Hematology, John Wiley & Sons, Incorporate d, (ISBN 978-0-8138-0896-3, lire en ligne), p. 487]