
Back ثلاثي فلوريد الكلور Arabic تریفلورید کولور AZB Trifluorur de clor Catalan Fluorid chloritý Czech Klortrifluorid Danish Chlortrifluorid German Τριφθοριούχο χλώριο Greek Chlorine trifluoride English Trifluoruro de cloro Spanish تریفلورید کلر Persian
| Trifluorure de chlore | |
   |
|
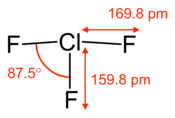
| Structure du trifluorure de chlore. | |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.029.301 |
| No CE | 232-230-4 |
| No RTECS | FO2800000 |
| PubChem | 24637 |
| ChEBI | 30123 |
| SMILES | |
| InChI | |
| Apparence | Gaz ou liquide jaunâtre |
| Propriétés chimiques | |
| Formule | ClF3 |
| Masse molaire[2] | 92,448 ± 0,002 g/mol Cl 38,35 %, F 61,65 %, |
| Moment dipolaire | 0,6 ± 0,1 D[1] |
| Propriétés physiques | |
| T° fusion | −76,31 °C[3] |
| T° ébullition | 11,8 °C[3] |
| Masse volumique | 3,57 kg·m-3[3] à 0 °C et 101,3 kPa |
| Pression de vapeur saturante | 141,9 kPa[3] à 20 °C |
| Point critique | 174,0 °C ; 5,78 MPa ; 0,548 g·cm-3[3] |
| Point triple | −76,3 °C[3] |
| Thermochimie | |
| ΔvapH° | 27,53 kJ·mol-1 (1 atm, 11,75 °C)[4] |
| Précautions | |
| SGH[3] | |
| H270, H280, H314, H330, H370, H372 et H400 |
|
| Transport[3] | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le trifluorure de chlore est un interhalogène de formule ClF3. C'est un gaz incolore, très oxydant et extrêmement réactif, corrosif et toxique, qui se condense en un liquide jaune verdâtre. C'est sous sa forme liquide pressurisée à température ambiante qu'on le trouve le plus souvent sur le marché. On s'en sert surtout dans les phases de nettoyage et pour les gravures chimiques dans l'industrie des semiconducteurs[5],[6], et dans quelques autres processus industriels[7]. Il est notamment utilisé dans le cycle du combustible nucléaire[8], où il permet la conversion des composés fluorés d'uranium non volatils en hexafluorure d'uranium UF6, composé aux propriétés physiques intéressantes du point de vue des procédés d'enrichissement de l'uranium :
Son utilisation comme comburant pour la propulsion spatiale est aujourd'hui abandonnée compte tenu des risques réels pour le matériel et pour les équipages ; c'est en revanche la matière première pour la synthèse du pentafluorure de chlore ClF5, un ergol parfois employé, le plus souvent avec l'hydrazine, pour la propulsion de certains missiles[9].
- (en) David R. Lide, Handbook of chemistry and physics, Boca Raton, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1 et 1-4200-6679-X), p. 9-50.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée « Chlorotrifluoride » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 27 mai 2018 (JavaScript nécessaire)
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, , 90e éd., 2804 p., Relié (ISBN 978-1-4200-9084-0).
- (en) Hitoshi Habuka, Takahiro Sukenobu, Hideyuki Koda, Takashi Takeuchi, and Masahiko Aihara, « Silicon Etch Rate Using Chlorine Trifluoride », Journal of the Electrochemical Society, vol. 151, no 11, , G783–G787 (DOI 10.1149/1.1806391).
- United States Patent 5849092 "Process for chlorine trifluoride chamber cleaning".
- United States Patent 6034016 "Method for regenerating halogenated Lewis acid catalysts".
- (en) (BEST) Board on Environmental Studies and Toxicology, Acute Exposure Guideline Levels for Selected Airborne Chemicals : Volume 5 http : //books.nap.edu/catalog.php?record_id=11774 (citation at the National Academies Press), Washington, National Academies Press, , 267 p., poche (ISBN 978-0-309-10358-9, LCCN 2002275572), p. 40.
- notamment certains missiles balistiques intercontinentaux, qui utilisent généralement des propergols liquides à quelques exceptions près, telles que, semble-t-il, le nouveau Jéricho-3 israélien.






