
Back تيروسين Arabic تيروسين ARZ تیروزین AZB Тирозин Bulgarian Tirozin BS Tirosina Catalan Tyrosin Czech Tyrosin Danish Tyrosin German Τυροσίνη Greek
| Tyrosine | |
 L ou S(–)-tyrosine 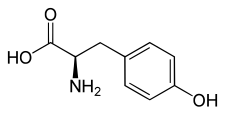 D ou R(+)-tyrosine |
|
| Identification | |
|---|---|
| Nom UICPA | acide (S)-2-amino-3-(4-hydroxyphényl)propanoïque |
| Synonymes |
Y, Tyr |
| No CAS | (racémique) (L) ou S(–) (D) ou R |
| No ECHA | 100.000.419 |
| No CE | 200-460-4 |
| DrugBank | DB00135 |
| PubChem | 6057 |
| ChEBI | 18186 |
| FEMA | 3736 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C9H11NO3 [Isomères] |
| Masse molaire[2] | 181,188 5 ± 0,009 1 g/mol C 59,66 %, H 6,12 %, N 7,73 %, O 26,49 %, |
| pKa | 2,2 pour l'acide ; 9,11 pour la base et 10,07 pour le groupement phénol [1] |
| Propriétés physiques | |
| T° fusion | 343 °C (décomposition) [1] |
| Solubilité | 479 mg·l-1 (eau,25 °C) [1] |
| Thermochimie | |
| S0solide | 214,01 J·mol-1·K-1 [3] |
| ΔfH0solide | −685,6 kJ·mol-1 [3] |
| Cp | 216,44 J·mol-1·K-1 (solide,25 °C)[3] |
| Propriétés biochimiques | |
| Codons | UAU, UAC |
| pH isoélectrique | 5,66[4] |
| Acide aminé essentiel | selon les cas |
| Occurrence chez les vertébrés | 3,3 %[5] |
| Précautions | |
| SIMDUT[6] | |
Produit non contrôlé |
|
| Écotoxicologie | |
| LogP | -2.26 [1] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
La tyrosine (abréviations IUPAC-IUBMB : Tyr et Y) est un acide α-aminé dont l'énantiomère L est l'un des 22 acides aminés protéinogènes, codé sur les ARN messagers par les codons UAU et UAC. Sa chaîne latérale comporte un groupe phénol dont l'hydroxyle est légèrement acide (pKa = 9,76[7]). Cet acide aminé n'est pas essentiel chez les mammifères mais peut néanmoins être produit en quantité insuffisante par l'organisme dans certains cas particuliers, nécessitant alors un apport alimentaire.
La tyrosine participe à la synthèse des catécholamines : l'adrénaline, la noradrénaline, la dopamine et la DOPA. Elle est aussi précurseur de la mélanine (pigment qui colore la peau, les poils, l'iris) et des hormones thyroïdiennes (formation de thyronine à partir de deux tyrosines).
- (en) « Tyrosine », sur ChemIDplus, consulté le 8 juillet 2009
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Tyrosine », sur NIST/WebBook, consulté le 8 juillet 2009
- (en) Francis A. Carey, « Table of pKa and pI values », sur Département de chimie de l'université de Calgary, (consulté le ).
- (en) M. Beals, L. Gross, S. Harrell, « Amino Acid Frequency », sur The Institute for Environmental Modeling (TIEM) à l'université du Tennessee (consulté le ).
- « Tyrosine (l-) » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- (en) Gerald Platzer, Mark Okon et Lawrence P. McIntosh, « pH-dependent random coil 1H, 13C, and 15N chemical shifts of the ionizable amino acids: a guide for protein pK a measurements », Journal of Biomolecular NMR, vol. 60, nos 2-3, , p. 109–129 (ISSN 0925-2738 et 1573-5001, DOI 10.1007/s10858-014-9862-y, lire en ligne, consulté le )