
Back جلوتامين Arabic Qlutamin Azerbaijani قلوتامین AZB Глутамин Bulgarian গ্লুটামিন Bengali/Bangla Glutamin BS Glutamina Catalan Glutamin Czech Glutamin Danish Glutamin German
| L-Glutamina | |
|---|---|
 | |
 | |
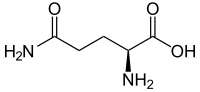
Glutamina | |
Outros nomes L-Glutamina | |
| Identificadores | |
| Abreviaturas | Gln, Q |
| Número CAS | 56-85-9 |
| PubChem | 738 |
| ChemSpider | 718 |
| UNII | 0RH81L854J |
| Número CE | 200-292-1 |
| KEGG | C00303 |
| ChEBI | CHEBI:28300 |
| ChEMBL | CHEMBL930 |
| Ligando IUPHAR | 723 |
| Código ATC | A16 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades[1] | |
| Fórmula molecular | C5H10N2O3 |
| Masa molar | 146,14 g mol−1 |
| Punto de fusión | descomponse arredor de 185 °C |
| Solubilidade en auga | soluble |
| Rotación quiral [α]D | +6,5º (H2O, c = 2) |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |


A glutamina (abreviadamente Gln ou Q) é un α-aminoácido que forma parte das proteínas (aminoácido proteinoxénico). A súa cadea lateral -CH2-CH2-CO-NH2 é unha amida formada ao substituír o grupo hidroxilo da cadea lateral do ácido glutámico por un grupo amino. Por tanto, pode considerarse como a amida do ácido glutámico cun grupo carboxiamida. O grupo amino é polar, polo que se considera un aminoácido polar neutro a pH celular. Nas proteínas aparece o isómero L.
Non se considera un aminoácido esencial, pero pode chegar a ser condicionalmente esencial en certas situacións, como adestramento atlético intenso ou trastornos gastrointestinais. Está codificado polos codóns do código xenético CAA e CAG. No sangue humano a glutamina é o aminoácido máis abundante, cunha concentración de arredor 500-900 µmol/L.[2]
Na súa degradación oxidativa a glutamina orixina alfa-cetoglutarato, que pode entrar na gliconeoxénese, polo que é un aminoácido glicoxénico.
- ↑ Weast, Robert C., ed. (1981). CRC Handbook of Chemistry and Physics (62nd ed.). Boca Raton, FL: CRC Press. p. C-311. ISBN 0-8493-0462-8.
- ↑ Brosnan John T. (2003). "Interorgan amino acid transport and its regulation". J. Nutr. 133 (6): 2068S–72S. PMID 12771367..