
Back Imidasool Afrikaans إيميدازول Arabic İmidazol Azerbaijani ایومیدازول AZB Імідазол Byelorussian Imidazol BS Imidazole Catalan Imidazol Czech Imidazol German Ιμιδαζόλιο Greek
| Imidazol | |
|---|---|

|

|
|

|
 | |
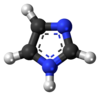
1H-Imidazol | |
Outros nomes 1,3-diazol | |
| Identificadores | |
| Número CAS | 288-32-4 |
| PubChem | 795 |
| ChemSpider | 773 |
| Número CE | 206-019-2 |
| KEGG | C01589 |
| ChEBI | CHEBI:16069 |
| ChEMBL | CHEMBL540 |
| Número RTECS | NI3325000 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | C3H4N2 |
| Masa molecular | 68,077 g/mol |
| Aspecto | sólido branco ou amarelo claro |
| Densidade | 1,23 g/cm3, sólido |
| Punto de fusión | 89–91 °C; 192–196 °F; 362–364 K |
| Punto de ebulición | 256 °C; 493 °F; 529 K |
| Solubilidade en auga | 633 g/L |
| Acidez (pKa) | 6,95 (para o ácido conxugado) [1] |
| λmax | 206 nm |
| Estrutura | |
| Estrutura cristalina | monoclínico |
| anel de 5 membros plano | |
| Momento dipolar | 3,61 D |
| Perigosidade | |
| declaración de perigosidade GHS | 302, 314, 360, 360D |
| declaración de precaución GHS | 201, 280, 305+351+338, 310, 330 [2] |
| Principais perigos | Corrosivo |
| Punto de inflamabilidade | 146 °C; 295 °F; 419 K |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
O imidazol é un composto orgánico coa fñormula C3N2H4. É un sólido branco ou incoloro soluble en auga, que produce unha disolución medianamente alcalina. En química, é un composto heterocíclico aromático, clasificado como un diazol e ten átomos de nitróxeno non adxacentes.
Moitos produtos naturais, especialmente alcaloides, conteñen o anel imidazol. Estes imidazois comparten o anel 1,3-C3N2 pero presentan diversos substituíntes. Este sistema anular está presente en importantes moléculas biolóxicas, como o aminoácido histidina e a hormona relacionada histamina. Moitos fármacos conteñen o anel imidazol, como certos antifúnxicos, a serie de antibióticos de nitroimidazol e o sedante midazolam.[3][4][5][6][7]
Cando se fusiona cun anel de pirimidina, forma unha purina, que é o composto heterocíclico que contén nitróxeno máis abondoso na natureza.[8]
O nome "imidazol" (imidazole) foi acuñado en 1887 polo químico alemán Arthur Rudolf Hantzsch (1857–1935).[9]
- ↑ Walba, H.; Isensee, R. W. (1961). "Acidity constants of some arylimidazoles and their cations". J. Org. Chem. 26 (8): 2789–2791. doi:10.1021/jo01066a039.
- ↑ "Imidazole".
- ↑ Karitzky, A. R.; Rees (1984). Comprehensive Heterocyclic Chemistry 5. pp. 469–498.
- ↑ Grimmett, M. Ross (1997). Imidazole and Benzimidazole Synthesis. Academic Press.
- ↑ Brown, E. G. (1998). Ring Nitrogen and Key Biomolecules. Kluwer Academic Press.
- ↑ Pozharskii, A. F.; et al. (1997). Heterocycles in Life and Society. John Wiley & Sons.
- ↑ Gilchrist, T. L. (1985). Heterocyclic Chemistry. Bath Press. ISBN 978-0-582-01421-3.
- ↑ Rosemeyer, H. (2004). "The Chemodiversity of Purine as a Constituent of Natural Products". Chemistry & Biodiversity 1 (3): 361–401. PMID 17191854. doi:10.1002/cbdv.200490033.
- ↑ Hantzsch, A. and Weber, J. H. (1887) "Ueber Verbindungen des Thiazols (Pyridins der Thiophenreihe)" (Sobre os compostos de tiazol (piridinas da serie do tiofeno), Berichte der deutschen chemischen Gesellschaft, 20 : 3118–3132, see p. 3119. Ver tamén: Hantzsch, A. (1888) "Allegemeine Bemerkungen über Azole" (Observacións xerais sobre os azois), Annalen der Chemie, 249 : 1–6. Hantzsch propuxo unha reforma da nomenclatura dos compostos de azol, incluíndo unha proposta para chamar o anel heterocíclico C3H3(NH)N "imidazole" ; ver pp. 2 e 4.