
Back Formaldehied Afrikaans ميثانال Arabic Formaldehídu AST Formaldehid Azerbaijani فرمالدهید AZB Фармальдэгід Byelorussian Формалдехид Bulgarian ফরমালিন Bengali/Bangla Formaldehid BS Formaldehid Catalan
| Formaldeide | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| formaldeide (preferito)
metanale (sistematico) | |
| Nomi alternativi | |
| aldeide fòrmica formalina | |
| Caratteristiche generali | |
| Formula bruta o molecolare | CH2O |
| Massa molecolare (u) | 30,03 |
| Aspetto | gas incolore |
| Numero CAS | |
| Numero EINECS | 200-001-8 |
| PubChem | 712 |
| DrugBank | DBDB03843 |
| SMILES | C=O |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,13 (a −19 °C) |
| Temperatura di fusione | −116,9 °C (156,2 K) |
| Temperatura di ebollizione | −19,0 °C (254,1 K) |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | −108,6 |
| ΔfG0 (kJ·mol−1) | −102,5 |
| S0m(J·K−1mol−1) | 218,8 |
| C0p,m(J·K−1mol−1) | 35,4 |
| Indicazioni di sicurezza | |
| Punto di fiamma | −53 °C (220 K) |
| Limiti di esplosione | 7 - 73% vol. |
| Temperatura di autoignizione | 430 °C (703 K) |
| Simboli di rischio chimico | |
    
| |
| pericolo | |
| Frasi H | 350 - 341 - 301 - 311 - 331 - 314 - 317 |
| Consigli P | 301+310 - 303+361+353 - 305+351+338 - 320 - 361 - 405 - 501 [1] |
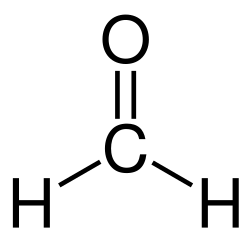
La formaldeide (o aldeide fòrmica, nome IUPAC: metanale) è un composto organico la cui formula molecolare è CH2O. Si tratta dell'aldeide più semplice, composta dal gruppo funzionale carbonilico (C=O) e due atomi di idrogeno.[2] Strutturalmente può essere rappresentata anche così: H2C=O.[3] A pressione e temperatura ambiente, si presenta come un gas incolore,[4] dal caratteristico odore pungente e fortemente irritante.[5]
A causa della mancanza di un gruppo funzionale alchilico (−R) legato al carbonile, come invece accade per tutte le altre aldeidi (R−CHO) e per tutti gli altri chetoni (R2−CO), la formaldeide ha delle significative differenze di reattività.[6]
Rientra nel gruppo 1 delle sostanze classificate dall'Agenzia internazionale per la ricerca sul cancro (IARC) in quanto ha mostrato evidenze di cancerogenicità per l'uomo.[7]
- ^ scheda della formaldeide in soluzione acquosa al 25% su IFA-GESTIS (archiviato dall'url originale il 16 ottobre 2019).
- ^ CHAPTER 1. Introduction to Formaldehyde, Royal Society of Chemistry, 2018, pp. 1–19, DOI:10.1039/9781788010269-00001, ISBN 978-1-78262-973-3. URL consultato il 17 febbraio 2024.
- ^ (EN) Aldehyde | Definition, Structure, Examples, & Facts | Britannica, su www.britannica.com, 26 agosto 2024. URL consultato il 18 ottobre 2024.
- ^ GESTIS-Stoffdatenbank, su gestis.dguv.de. URL consultato il 17 febbraio 2024.
- ^ (EN) PubChem, Formaldehyde, su pubchem.ncbi.nlm.nih.gov. URL consultato il 27 luglio 2022.
- ^ R.O.C. Norman, CHIMICA ORGANICA Principi e Applicazioni alla Sintesi, traduzione di Paolo Da Re, Piccin, 1973, p. 566.
- ^ Errore nelle note: Errore nell'uso del marcatore
<ref>: non è stato indicato alcun testo per il marcatore:2