
Back Koolstofdisulfied Afrikaans ثنائي كبريتيد الكربون Arabic Karbon disulfid Azerbaijani کربون دیسولفید AZB Серавуглярод Byelorussian Серкавуглярод BE-X-OLD Въглероден дисулфид Bulgarian Sulfur de carboni Catalan Sirouhlík Czech Кӳкĕртле кăмрăкамăш CV
| Solfuro di carbonio | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| disolfuro di carbonio | |
| Caratteristiche generali | |
| Formula bruta o molecolare | CS2 |
| Massa molecolare (u) | 76,14 g/mol |
| Aspetto | liquido incolore |
| Numero CAS | |
| Numero EINECS | 200-843-6 |
| PubChem | 6348 |
| SMILES | C(=S)=S |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,26 (20 °C) |
| Solubilità in acqua | 2,1 g/l (20 °C) |
| Temperatura di fusione | −111 °C (162 K) |
| Temperatura di ebollizione | 47 °C (320 K) |
| Indicazioni di sicurezza | |
| Punto di fiamma | −30 °C (243 K) |
| Limiti di esplosione | 1 - 60 Vol% |
| Temperatura di autoignizione | 100 °C (373 K) |
| Simboli di rischio chimico | |
   
| |
| pericolo | |
| Frasi H | 225 - 302 - 315 - 319 - 361 - 372 - 412 |
| Consigli P | 201 - 210 - 273 - 280 - 308+313 - 337+313 [1] |
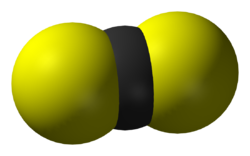
Il solfuro di carbonio (nome sistematico: disolfuro di carbonio) è un composto binario del carbonio tetravalente con lo zolfo, avente formula molecolare CS2.
La sua molecola è isoelettronica di valenza con l'anidride carbonica e, in analogia a quest'ultima, CS2 è considerato la tioanidride dell'acido tiocarbonico H2CS3, composto instabile al pari dell'acido carbonico H2CO3,[2] e dal quale derivano i corrispondenti tiosali, importanti in chimica analitica qualitativa.[3]
A temperatura ambiente il solfuro di carbonio si presenta come un liquido incolore molto volatile (Teb. = 46,25 °C) e infiammabile, dall'odore etereo piacevole[4] che ricorda in parte quello dolce del cloroformio.[5][6] Al contrario, in campioni commerciali non purissimi presenta un caratteristico odore sgradevole.[5]
È un composto irritante e tossico a causa della sua interazione con il sistema nervoso centrale, come pure COS,[7] e nocivo alla riproduzione.[4]
È tuttavia un ottimo solvente, ottimo per cere, grassi, idrocarburi e sostanze non polari in genere;[8] è inoltre il migliore conosciuto per elementi puri quali zolfo elementare e fosforo bianco (P4).
- ^ scheda del solfuro di carbonio su IFA-GESTIS
- ^ trithiocarbonic acid, su webbook.nist.gov.
- ^ G. Gioia Lobbia e G. Novara, ANALISI QUALITATIVA E COMPLEMENTI DI CHIMICA, Bulgarini, 1988, p. 456.
- ^ a b N. N. Greenwood e A. Earnshaw, Chemistry of the Elements, 2ª ed., Butterworth - Heinemann, 1997, pp. 317-318, ISBN 0-7506-3365-4.
- ^ a b (EN) Is CS2 Ionic or Covalent? - Techiescientist, su techiescientist.com, 18 settembre 2021. URL consultato il 28 ottobre 2024.
- ^ Carbon disulfide | CS2, su chemspider.com. URL consultato il 28 ottobre 2024.
- ^ Nils Wiberg, Egon Wiberg e Arnold Frederik Holleman, Anorganische Chemie, 103. Auflage, De Gruyter, 2017, p. 1040, ISBN 978-3-11-026932-1.
- ^ Therald Moeller, John C. Bailar, Jr. e Jacob Kleinberg, Chemistry with inorganic qualitative analysis, Academic Press, 1980, p. 718, ISBN 978-0-12-503350-3.