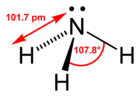Back Ammoniak Afrikaans أمونيا Arabic أمونياك ARY এম’নিয়া Assamese Amoniacu AST Ammonyak Azerbaijani آمونیاک AZB Amonya BCL Аміяк Byelorussian Аміяк BE-X-OLD
| |||||||||||||||||||||||||||||||||||||||||
 butla ze sprężonym amoniakiem | |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny |
NH | ||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
17,03 g/mol | ||||||||||||||||||||||||||||||||||||||||
| Wygląd |
bezbarwny gaz o charakterystycznym drażniącym zapachu | ||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||
| DrugBank | |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||||||||
| Inne aniony | |||||||||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||||||||
| Pochodne | |||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||||||||||||||||
Amoniak (nazwy systematyczne: azan, trihydrydoazot[1]), NH
3 – nieorganiczny związek chemiczny azotu i wodoru.
- ↑ a b c d Błąd w przypisach: Błąd w składni elementu
<ref>. Brak tekstu w przypisie o nazwieRedBookBŁĄD PRZYPISÓW - ↑ a b c d e Lide 2009 ↓, s. 4-46.
- ↑ Lide 2009 ↓, s. 8-40.
- ↑ a b Lide 2009 ↓, s. 6-51.
- ↑ Lide 2009 ↓, s. 9-51.
- ↑ a b Amoniak, [w:] Classification and Labelling Inventory, Europejska Agencja Chemikaliów [dostęp 2015-04-10] (ang.).
- ↑ a b Błąd w przypisach: Błąd w składni elementu
<ref>. Brak tekstu w przypisie o nazwieSABŁĄD PRZYPISÓW