
Back Хіральнасць Byelorussian Хиралност Bulgarian Chiralita Czech Chirality English Quiralidad Spanish Kiraalsus Estonian Kiralitate Basque دستسانی Persian Chiralité French Quiralidade Galician
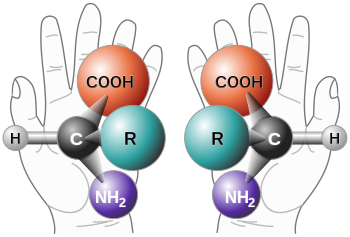
Hiralnost (grč. χειρ – kheir = ruka) svojstvo je simetrije koje je važno u nekoliko grana nauke.
Objekt ili sistem je hiralan ako se njegovi oblici razlikuju od svojih slika u ogledalu, tj. ne mogu biti međusobno superponirani. Nasuprot tome, izgled u ogledalu ahiralnog predmeta, kao što je sferični, ne može se razlikovati od objekta. Hiralni objekti i njihove slike u ogledalu se nazivaju enantiomorfi (grč. = suprotnost forme) ili enantiomeri kada se odnosi na molekule. Nehiralni predmeti zovu se ahiralni (ponekad i amfihiralni) i mogu se superponirati na odraz u ogledalu.
Ako je objekt nehiralni i zamisli se kao da je plava, onda se njegova slika u ogledalu zamišlja kao da je žuta. Zatim se nizom rotacija i translacija ove dvije boje mogu biti preklopljene, ne dajući zeleno ni s jednom od preostalih originalnih boja.
Hiralnost / nehiralnost još očitije ilustrira poređenje zavrtnja i eksera. Prvi ima lijeve ili desne navoje, a drugi nema nikakve.[1][2][3][4]
Izraz hiralnost prvi je put koristio lord Kelvin 1893. na predavanju u Oxford University Junior Scientific Clubu, koje je objavljeno 1894. godine.[5]
Strane ljudskog tijela su možda najčešće općepriznati primjer hiralnosti: lijeva ruka je supernepoklapajući odraz desnoj; bez obzira na to koliko su orijentirane dvije ruke, nemoguće ih je poklopiti tako da se sve glavne osobine obje podudare u svim pravcima. Ova razlika u simetriji postaje jasna ako se neko pokuša rukovati s desne strane ili ako rukavicu lijeve ruke stavi na desnu. U matematici hiralnost je u području brojki koje nisu identične svom odrazu u ogledalu.
- ^ Atkins P., de Paula J. (2006): Physical chemistry, 8th Ed. W. H. Freeman, San Francisco, ISBN 0-7167-8759-8
- ^ Binder H. H. (1999): Lexikon der chemischen Elemente. S. Hirzel Verlag, Stuttgart, ISBN 3-7776-0736-3.
- ^ Whitten K.W., Gailey K. D. and Davis R. E. (1992): General chemistry, 4th Ed. Saunders College Publishing, Philadelphia, ISBN 0-03-072373-6.
- ^ Petrucci R.H., Harwood W.S. and Herring F.G. (2002): General Chemistry, 8th Ed. Prentice-Hall, New York, ISBN 0-13-014329-4.
- ^ Sir William Thomson Lord Kelvin (1894): The molecular tactics of a crystal. Clarendon Press: http://archive.org/details/moleculartactic00kelvgoog.